Vedecký pokrok v oblasti environmentálnej toxikológie a genetiky nám postupne odhaľuje komplexné vzťahy medzi vonkajšími faktormi a naším vnútorným biologickým systémom. Dojčiakova Open Reality sa snaží zmapovať tieto súvislosti, pričom sa zameriava na potenciálne škodlivé environmentálne látky, ako je nikiel, a na genetické predispozície k rôznym ochoreniam. Tento rozsiahly prehľad sa ponorí do molekulárnych mechanizmov toxicity niklu, genetických základov alergických ochorení, rastových procesov, neurodegeneratívnych chorôb a vplyvu genetických variácií na niektoré fyziologické reakcie.
Nikel ako environmentálny toxín a jeho molekulárne dopady
Nickel is a potent environmental pollutant in industrial countries. Because nickel compounds are carcinogenic, exposure to nickel represents a serious hazard to human health. The understanding of how nickel exerts its toxic and carcinogenic effects at a molecular level may be important in risk assessment, as well as in the treatment and prevention of occupational diseases. Previously, using human and rodent cells in vitro, we showed that hypoxia-inducible signaling pathway was activated by carcinogenic nickel compounds. Acute exposure to nickel resulted in the accumulation of hypoxia-inducible transcription factor (HIF)-1, which strongly activated hypoxia-inducible genes, including the recently discovered tumor marker NDRG1 (Cap43). To further identify HIF-1-dependent nickel-inducible genes and to understand the role of the HIF-dependent signaling pathway in nickel-induced transformation, we used the Affymetrix GeneChip to compare the gene expression profiles in wild-type cells or in cells from HIF-1 alpha knockout mouse embryos exposed to nickel chloride. As expected, when we examined 12,000 genes for expression changes, we found that genes coding for glycolytic enzymes and glucose transporters, known to be regulated by HIF-1 transcription factor, were induced by nickel only in HIF-1 alpha-proficient cells. In addition, we found a number of other hypoxia-inducible genes up-regulated by nickel in a HIF-dependent manner including BCL-2-binding protein Nip3, EGLN1, hypoxia-inducible gene 1 (HIG1), and prolyl 4-hydroxylase. Additionally, we found a number of genes induced by nickel in a HIF-independent manner, suggesting that Ni activated other signaling pathways besides HIF-1. Finally, we found that in HIF-1 alpha knockout cells, nickel strongly induced the expression of the whole group of genes that were not expressed in the presence of HIF-1. Because the majority of modulated genes were induced or suppressed by nickel in a HIF-1-dependent manner, we elucidated the role of HIF-1 transcription factor in cell transformation. In HIF-1 alpha-proficient cells, nickel exposure increased soft agar growth, whereas it decreased soft agar growth in HIF-1 alpha-deficient cells.
Tieto zistenia poukazujú na komplexnú odpoveď buniek na expozíciu niklu. Aktivácia hypoxiou indukovateľného faktora (HIF-1) v prítomnosti karcinogénnych zlúčenín niklu je kľúčovým mechanizmom, ktorý spúšťa kaskádu génových expresií. HIF-1 je transkripčný faktor, ktorý hrá zásadnú úlohu v bunkovej adaptácii na nízke hladiny kyslíka (hypoxiu), ale ako sa ukazuje, je tiež aktivovaný environmentálnymi toxínmi. V reakcii na nikol sa v bunkách akumuluje HIF-1, čo vedie k silnej aktivácii génov regulovaných týmto faktorom. Medzi tieto gény patrí napríklad NDRG1 (známy ako tumor marker Cap43), ktorý je dôležitý pri bunkovej transformácii.
Štúdie pomocou microarray technológie (Affymetrix GeneChip) na porovnanie génových expresných profilov voľne žijúcich typov buniek a buniek z embryí myší s deficienciou HIF-1 alfa (knockout) vystavených chloridu nikelnému, priniesli detailnejšie informácie. Bolo identifikovaných 12 000 génov, u ktorých sa sledovali zmeny expresie. Výsledky potvrdili, že gény kódovacie pre glykolytické enzýmy a glukózové transportéry, ktoré sú známe ako regulované transkripčným faktorom HIF-1, boli indukované niklom len v bunkách s prítomnosťou HIF-1 alfa. Okrem toho boli v HIF-1 dependentnom mechanizme objavené ďalšie hypoxiou indukovateľné gény, ako napríklad Nip3 (BCL-2-binding protein), EGLN1, HIG1 (hypoxia-inducible gene 1) a prolyl 4-hydroxyláza.
Zaujímavé je, že boli identifikované aj gény, ktoré boli indukované niklom nezávisle od HIF-1, čo naznačuje, že nikol aktivuje aj iné signálne dráhy okrem HIF-1. Tieto zistenia naznačujú, že vplyv niklu na bunkovú signalizáciu je mnohostranný a zahŕňa viacero regulačných mechanizmov.
Ďalším kľúčovým zistením bolo, že v bunkách s deficienciou HIF-1 alfa nikol silno indukoval expresiu celej skupiny génov, ktoré v prítomnosti HIF-1 neboli exprimované. Toto naznačuje, že HIF-1 môže mať aj represívnu úlohu pri expresii niektorých génov v reakcii na nikol. Keďže väčšina modifikovaných génov bola indukovaná alebo potlačená niklom v závislosti od HIF-1, bola objasnená úloha tohto transkripčného faktora v bunkovej transformácii. V bunkách s prítomnosťou HIF-1 alfa expozícia niklu zvýšila rast v mäkkom agare (soft agar growth), čo je in vitro metrika pre bunkovú transformáciu a potenciálnu karcinogenitu. Naopak, v bunkách s deficienciou HIF-1 alfa sa rast v mäkkom agare znížil. Tieto výsledky jednoznačne poukazujú na kritickú úlohu HIF-1 v mechanizmoch karcinogénneho účinku niklu.
HOW MERCURY IS PRODUCED ☣️ | The MOST TOXIC METAL on the PLANET 💀
Genetické základy alergických ochorení
Asthma, hay fever (or allergic rhinitis) and eczema (or atopic dermatitis) often coexist in the same individuals, partly because of a shared genetic origin. To identify shared risk variants, we performed a genome-wide association study (GWAS; n = 360,838) of a broad allergic disease phenotype that considers the presence of any one of these three diseases. We identified 136 independent risk variants (P < 3 × 10 -8 ), including 73 not previously reported, which implicate 132 nearby genes in allergic disease pathophysiology. Disease-specific effects were detected for only six variants, confirming that most represent shared risk factors. Tissue-specific heritability and biological process enrichment analyses suggest that shared risk variants influence lymphocyte-mediated immunity. Six target genes provide an opportunity for drug repositioning, while for 36 genes CpG methylation was found to influence transcription independently of genetic effects. Asthma, hay fever (or allergic rhinitis) and eczema (or atopic dermatitis) often coexist in the same individuals1, partly because of a shared genetic origin2-4. To identify shared risk variants, we performed a genome-wide association study (GWAS, n=360,838) of a broad allergic disease phenotype that considers the presence of any one of these three diseases. We identified 136 independent risk variants (P<3x10-8), including 73 not previously reported, which implicate 132 nearby genes in allergic disease pathophysiology. Disease-specific effects were detected for only six variants, confirming that most represent shared risk factors. Tissue-specific heritability and biological process enrichment analyses suggest that shared risk variants influence lymphocyte-mediated immunity. Six target genes provide an opportunity for drug repositioning, while for 36 genes CpG methylation was found to influence transcription independently of genetic effects. Asthma, hay fever and eczema partly coexist because they share many genetic risk variants that dysregulate the expression of immune-related genes.
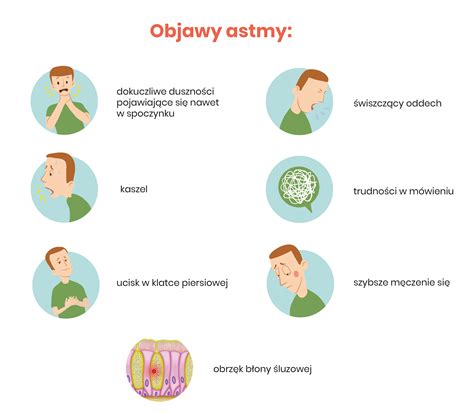
Súbežný výskyt astmy, sennnej nádchy (alergickej rhinitídy) a ekzému (atopickej dermatitídy) u tých istých jedincov nie je náhodný. Existuje čiastočne spoločná genetická predispozícia, ktorá ovplyvňuje ich vznik. Na identifikáciu týchto spoločných rizikových variantov bola vykonaná rozsiahla genómová asociačná štúdia (GWAS) zahŕňajúca 360 838 účastníkov. Štúdia sa zamerala na široký fenotyp alergických ochorení, ktorý zohľadňoval prítomnosť ktorejkoľvek z týchto troch chorôb.
Výsledkom bolo identifikovaných 136 nezávislých rizikových variantov (s pravdepodobnosťou P < 3 × 10⁻⁸), z ktorých 73 nebolo doteraz známych. Tieto varianty poukazujú na 132 blízkych génov, ktoré sa podieľajú na patofyziológii alergických ochorení. Bolo zistené, že len šesť variantov malo špecifické účinky pre jednotlivé choroby, čo potvrdzuje, že väčšina z nich predstavuje spoločné rizikové faktory. Analýzy tkanivovo-špecifickej dedičnosti a obohatenia biologických procesov naznačujú, že spoločné rizikové varianty ovplyvňujú imunitu sprostredkovanú lymfocytmi. Šesť cieľových génov ponúka možnosť prekládky liekov (drug repositioning), zatiaľ čo u 36 génov sa zistilo, že metylácia CpG ovplyvňuje ich transkripciu nezávisle od genetických efektov. Tieto zistenia zdôrazňujú, že alergické ochorenia nie sú len výsledkom izolovaných genetických chýb, ale skôr komplexnou interakciou viacerých génov a environmentálnych faktorov, ktoré dysregulujú expresiu génov súvisiacich s imunitným systémom.
Genetické determinanty telesnej výšky
Using genome-wide data from 253,288 individuals, we identified 697 variants at genome-wide significance that together explained one-fifth of heritability for adult height. By testing different numbers of variants in independent studies, we show that the most strongly associated ~2,000, ~3,700 and ~9,500 SNPs explained ~21%, ~24% and ~29% of phenotypic variance. Furthermore, all common variants together captured the majority (60%) of heritability. The 697 variants clustered in 423 loci enriched for genes, pathways, and tissue-types known to be involved in growth and together implicated genes and pathways not highlighted in earlier efforts, such as signaling by fibroblast growth factors, WNT/beta-catenin, and chondroitin sulfate-related genes. We identified several genes and pathways not previously connected with human skeletal growth, including mTOR, osteoglycin and binding of hyaluronic acid. Our results indicate a genetic architecture for human height that is characterized by a very large but finite number (thousands) of causal variants.

Výška človeka je komplexný znak ovplyvnený mnohými génmi a environmentálnymi faktormi. Rozsiahle genómové štúdie, ktoré analyzovali dáta od viac ako 253 000 jedincov, identifikovali 697 variantov na úrovni genómovej signifikancie, ktoré spolu vysvetľujú približne pätinu dedičnosti telesnej výšky. Tieto zistenia boli ďalej potvrdené v nezávislých štúdiách, kde sa ukázalo, že najsilnejšie asociované SNP (jednovukleotidové polymorfizmy) - približne 2 000, 3 700 a 9 500 - vysvetlili 21 %, 24 % a 29 % fenotypovej variability. Celkovo všetky bežné varianty zachytili väčšinu (60 %) dedičnosti telesnej výšky.
Týchto 697 variantov sa zhlukuje do 423 génových lokusov, ktoré sú obohatené o gény, dráhy a typy tkanív známe tým, že sa podieľajú na raste. Tieto lokusy zároveň poukazujú na gény a dráhy, ktoré doteraz neboli v popredí výskumu, ako napríklad signalizácia fibroblastovými rastovými faktormi, WNT/beta-katenínová dráha a gény súvisiace s chondroitín sulfátom. Objavili sa aj gény a dráhy, ktoré doteraz neboli spojené s ľudským kostrovým rastom, vrátane mTOR, osteoglycínu a väzby kyseliny hyalurónovej. Tieto výsledky naznačujú, že genetická architektúra ľudskej výšky je charakterizovaná veľmi veľkým, ale konečným počtom (tisícky) kauzálnych variantov, ktoré prispievajú k tejto komplexnej vlastnosti.
Vplyv genetických variácií na únavu pri liečbe rakoviny prostaty
Fatigue is a common and distressing side effect of androgen deprivation therapy (ADT) for prostate cancer. The goal of the current study was to examine the relationship between changes in fatigue following initiation of ADT and single nucleotide polymorphisms (SNPs) in three pro-inflammatory cytokine genes: interleukin-1 beta (IL1B), interleukin-6 (IL6), and tumor necrosis factor alpha (TNFA). Methods As part of a larger study, men with prostate cancer (n=53) were recruited prior to initiation of ADT. Fatigue was assessed at recruitment and six months after initiation of ADT. DNA was extracted from blood drawn at baseline. Results Patients with the IL6-174 (rs1800795) G/C or C/C genotype displayed greater increases in fatigue intrusiveness, frequency, and duration than the G/G genotype (p valuesâ¤0.05), although inclusion of age, race, and baseline depressive symptomatology in the model attenuated these relationships (p valuesâ¤0.09). Patients with the TNFA-308 (rs1800629) G/A genotype showed greater increases in fatigue severity than the G/G genotype (p=0.02). IL1B-511 (rs16944) genotype did not significantly predict changes in fatigue (p values>0.46). Patients with higher numbers of variants displayed greater increases in fatigue duration and interference (p valuesâ¤0.02) than patients with lower numbers of variants. Conclusions Prostate cancer patients treated with ADT who carry variant alleles of the IL6 and TNFA genes are susceptible to heightened fatigue. These preliminary data lend support for the role of genetic variation in the development of cancer-related fatigue secondary to ADT. Findings are relevant to attempts to develop personalized approaches to cancer treatment.

Únava je častým a nepríjemným vedľajším účinkom liečby depriváciou androgénov (ADT) pri rakovine prostaty. Cieľom tejto štúdie bolo preskúmať vzťah medzi zmenami únavy po začatí ADT a jednovukleotidovými polymorfizmami (SNP) v troch pro-zápalových génoch cytokínov: interleukín-1 beta (IL1B), interleukín-6 (IL6) a faktor nádorovej nekrózy alfa (TNFA).
V rámci rozsiahlejšej štúdie bolo pred začatím ADT zaradených 53 mužov s rakovinou prostaty. Únavu hodnotili pri náборе a šesť mesiacov po začatí ADT. Z krvi odobratej v základnom stave bola extrahovaná DNA. Výsledky ukázali, že pacienti s genotypom IL6-174 (rs1800795) G/C alebo C/C vykazovali väčšie zvýšenie v intenzite, frekvencii a dĺžke únavy v porovnaní s genotypom G/G (p hodnota ≤ 0,05). Aj keď zahrnutie veku, rasy a základnej depresívnej symptomatológie do modelu tieto vzťahy oslabilo (p hodnota ≤ 0,09). Pacienti s genotypom TNFA-308 (rs1800629) G/A vykazovali väčšie zvýšenie v závažnosti únavy v porovnaní s genotypom G/G (p = 0,02). Genotyp IL1B-511 (rs16944) významne nepredikoval zmeny v únave (p hodnota > 0,46). Pacienti s vyšším počtom variantov vykazovali väčšie zvýšenie v dĺžke a interferencii únavy (p hodnota ≤ 0,02) v porovnaní s pacientmi s nižším počtom variantov.
Závery štúdie naznačujú, že pacienti s rakovinou prostaty liečení ADT, ktorí nesú variantné alely génov IL6 a TNFA, sú náchylnejší na zvýšenú únavu. Tieto predbežné údaje podporujú úlohu genetickej variability vo vývoji únavy súvisiacej s rakovinou, ktorá je sekundárna k ADT. Zistenia sú relevantné pre snahy o vývoj personalizovaných prístupov k liečbe rakoviny.
Genetické variácie a Alzheimerova choroba
Because currently known Alzheimer's disease (AD) single-nucleotide polymorphisms only account for a small fraction of the genetic variance in this disease, there is a need to identify new variants associated with AD. Our team performed a genome-wide association study in the Quebec Founder Population isolate to identify novel protective or risk genetic factors for late-onset sporadic AD and examined the impact of these variants on gene expression and AD pathology. The rs10984186 variant is associated with an increased risk of developing AD and with a higher CDK5RAP2 mRNA prevalence in the hippocampus. On the other hand, the rs4837766 variant, which is among the best cis-expression quantitative trait loci in the CDK5RAP2 gene, is associated with lower mild cognitive impairment/AD risk and conversion rate. The rs10984186 risk and rs4837766 protective polymorphic variants of the CDK5RAP2 gene might act as potent genetic modifiers for AD risk and/or conversion by modulating the expression of this gene.
V súčasnosti známe jednovukleotidové polymorfizmy (SNP) spojené s Alzheimerovou chorobou (AD) vysvetľujú len malú časť genetickej variability tejto choroby, čo poukazuje na potrebu identifikácie nových asociovaných variantov. Genómová asociačná štúdia (GWAS) vykonaná v Quebecskej zakladateľskej populácii izolovaného typu mala za cieľ identifikovať nové protektívne alebo rizikové genetické faktory pre sporadickú formu AD neskorého nástupu. Zároveň sa skúmal vplyv týchto variantov na génovú expresiu a patológiu AD.
Výsledky ukázali, že variant rs10984186 je spojený so zvýšeným rizikom rozvoja AD a s vyšším výskytom mRNA CDK5RAP2 v hipokampe. Na druhej strane, variant rs4837766, ktorý patrí medzi najlepšie cis-expresné kvantitatívne znaky v géne CDK5RAP2, je spojený s nižším rizikom mierneho kognitívneho poškodenia/AD a nižšou mierou konverzie. Tieto zistenia naznačujú, že rizikový polymorfný variant rs10984186 a protektívny polymorfný variant rs4837766 génu CDK5RAP2 môžu pôsobiť ako silné genetické modifikátory rizika AD a/alebo konverzie tým, že modulujú expresiu tohto génu. Tieto objavy sú dôležité pre pochopenie genetických mechanizmov Alzheimerovej choroby a pre vývoj cielenejších diagnostických a terapeutických stratégií.
Genetické mechanizmy v neurodegeneratívnych a psychiatrických poruchách
Serotonin (5-HT) receptors are 5-HT release-regulating autoreceptors in the human brain. Abnormalities in brain 5-HT function have been hypothesized in the pathophysiology of various psychiatric disorders, including obsessive-compulsive disorder, autism, mood disorders, eating disorders, impulsive violent behavior, and alcoholism. Thus, mutations occurring in 5-HT autoreceptors may cause or increase the vulnerability to any of these conditions. 5-HT1Dα and 5-HT1Dβ subtypes have been previously localized to chromosomes 1p36.3-p34.3 and 6q13, respectively, using rodent-human hybrids and in situ localization. In this communication, we report the detection of a 5-HT1Dα receptor gene polymorphism by single strand conformation polymorphism (SSCP) analysis of the coding sequence. The polymorphism was used for fine scale linkage mapping of 5-HT1Dα on chromosome 1. This polymorphism should also be useful for linkage studies in populations and in families. Our analysis also demonstrates that functionally significant coding sequence variants of the 5-HT1Dα are probably not abundant either among alcoholics or in the general population.
Substitution mutations adversely affecting the {alpha}-subunit of {beta}-hexosaminidase A ({alpha}{beta}) (EC 3.2.1.52) result in Tay-Sachs disease. The majority affect the initial folding of the pro-{alpha} chain in the endoplasmic reticulum, resulting in its retention and degradation. A much less common occurrence is a mutation that specifically affects an {openquotes}active-site{closequotes} residue necessary for substrate binding and/or catalysis. In this case, hexosaminidase A is present in the lysosome, but it lacks all {alpha}-specific activity. This biochemical phenotype is referred to as the {openquotes}B1-variant form{closequotes} of Tay-Sachs disease. Kinetic analysis of suspected B1-variant mutations is complex because hexosaminidase A is heterodimeric and bothmore » subunits possess similar active sites. In this report, we examine a previously identified B1-variant mutation, {alpha}-Val{sup 192}Leu. Chinese hamster ovary cells were permanently cotransfected with an {alpha}-cDNA-construct encoding the substitution and a mutant {beta}-cDNA ({beta}-Arg{sup 211}Lys), encoding a {beta}-subunit that is inactive but normal in all other respects. We were surprised to find that the Val{sup 192}Leu substitution produced a pro-{alpha} chain that did not form {alpha}-{beta} dimers and was not transported to the lysosome. Finally, we reexamined the hexosaminidase activity and protein levels in the fibroblasts from the original patient. These data were also not consistent with the biochemical phenotype of the B1 variant of Tay-Sachs disease previously reported to be present. Thus, we conclude that the Val{sup 192}Leu substitution does not specifically affect the {alpha}-active site.
Receptory pre serotonín (5-HT) v ľudskom mozgu fungujú ako autoreceptory regulujúce uvoľňovanie 5-HT. Abnormality v mozgových funkciách serotonínu boli hypoteticky spojené s patofyziológiou rôznych psychiatrických porúch, vrátane obsedantno-kompulzívnej poruchy, autizmu, porúch nálady, porúch príjmu potravy, impulzívneho násilného správania a alkoholizmu. Mutácie v autoreceptoroch 5-HT tak môžu spôsobiť alebo zvýšiť zraniteľnosť voči týmto stavom. Podtypy 5-HT1Dα a 5-HT1Dβ boli predtým lokalizované na chromozómoch 1p36.3-p34.3 a 6q13 pomocou potkaních-ľudských hybridov a in situ lokalizácie. V tejto práci bola detegovaná polymorfia génu receptora 5-HT1Dα pomocou analýzy konformačnej polymorfizmu jednovláknovej DNA (SSCP) kódovacej sekvencie. Táto polymorfia bola použitá na detailné mapovanie väzby 5-HT1Dα na chromozóm 1. Táto polymorfia by mala byť užitočná aj pre štúdie väzby v populáciách a rodinách. Analýza tiež ukazuje, že funkčne významné varianty kódovacej sekvencie 5-HT1Dα pravdepodobne nie sú hojne zastúpené ani medzi alkoholikmi, ani v bežnej populácii.
Substitučné mutácie nepriaznivo ovplyvňujúce α-podjednotku β-hexozaminidázy A (αβ) (EC 3.2.1.52) vedú k Tay-Sachsovej chorobe. Väčšina z nich ovplyvňuje počiatočné skladanie pro-α reťazca v endoplazmatickom retikule, čo vedie k jeho retencii a degradácii. Oveľa menej častým javom je mutácia, ktorá špecificky ovplyvňuje rezíduum v aktívnom centre nevyhnutné pre väzbu substrátu a/alebo katalýzu. V tomto prípade je hexozaminidáza A prítomná v lyzozóme, ale postráda všetku α-špecifickú aktivitu. Tento biochemický fenotyp sa označuje ako B1-variantná forma Tay-Sachsovej choroby. Kinetická analýza podozrivých B1-variantných mutácií je zložitá, pretože hexozaminidáza A je heterodimérna a obe podjednotky majú podobné aktívne centrá. V tejto správe skúmame predtým identifikovanú B1-variantnú mutáciu, α-Val¹⁹²Leu. Čínske vaječníkové bunky škrečka boli trvalo ko-transfektované s α-cDNA konštruktom kódujúcim substitúciu a s mutantnou β-cDNA (β-Arg²¹¹Lys), ktorá kóduje β-podjednotku, ktorá je neaktívna, ale vo všetkých ostatných ohľadoch normálna. Prekvapivo sme zistili, že substitúcia Val¹⁹²Leu produkovala pro-α reťazec, ktorý netvoril α-β diméry a nebol transportovaný do lyzozómu. Nakoniec sme znovu preskúmali aktivitu hexozaminidázy a hladiny proteínov vo fibroblastoch od pôvodného pacienta. Tieto údaje tiež neboli v súlade s biochemickým fenotypom B1 variantu Tay-Sachsovej choroby, ktorý bol predtým hlásený ako prítomný. Preto dochádzame k záveru, že substitúcia Val¹⁹²Leu špecificky neovplyvňuje α-aktívne centrum.
Metodika identifikácie kauzálnych variantov v asociovaných regiónoch
Motivation: Although genome-wide association studies (GWAS) have identified thousands of variants associated with common diseases and complex traits, only a handful of these variants are validated to be causal. We consider ‘causal variants’ as variants which are responsible for the association signal at a locus. As opposed to association studies that benefit from linkage disequilibrium (LD), the main challenge in identifying causal variants at associated loci lies in distinguishing among the many closely correlated variants due to LD. This is particularly important for model organisms such as inbred mice, where LD extends much further than in human populations, resulting in large stretches of the genome with significantly associated variants. Furthermore, these model organisms are highly structured and require correction for population structure to remove potential spurious associations. Results: In this work, we propose CAVIAR-Gene (CAusal Variants Identification in Associated Regions), a novel method that is able to operate across large LD regions of the genome while also correcting for population structure. A key feature of our approach is that it provides as output a minimally sized set of genes that captures the genes which harbor causal variants with probability ρ. Through extensive simulations, we demonstrate that our method not only speeds up computation, but also have an average of 10% higher recall rate compared with the existing approaches. We validate our method using a real mouse high-density lipoprotein data (HDL) and show that CAVIAR-Gene is able to identify Apoa2 (a gene known to harbor causal variants for HDL), while reducing the number of genes that need to be tested for functionality by a factor of 2. Availability and implementation: Software is freely available for download at genetics.cs.ucla.edu/caviar.
Hoci genómové asociačné štúdie (GWAS) identifikovali tisíce variantov spojených s bežnými chorobami a komplexnými znakmi, len hŕstka z týchto variantov je validovaná ako kauzálna. Kauzálne varianty sú tie, ktoré sú zodpovedné za asociačný signál na lokuse. Na rozdiel od asociačných štúdií, ktoré využívajú väzbovú nerovnováhu (LD), hlavnou výzvou pri identifikácii kauzálnych variantov na asociovaných lokusoch je rozlíšiť medzi mnohými úzko korelovanými variantmi v dôsledku LD. To je obzvlášť dôležité pre modelové organizmy, ako sú laboratórne myši, kde LD siaha oveľa ďalej ako v ľudských populáciách, čo vedie k rozsiahlym úsekom genómu s významne asociovanými variantmi. Navyše, tieto modelové organizmy sú vysoko štruktúrované a vyžadujú korekciu populácie, aby sa odstránili potenciálne falošné asociácie.
V tejto práci je predstavený CAVIAR-Gene (CAusal Variants Identification in Associated Regions), nová metóda, ktorá dokáže pracovať cez veľké LD regióny genómu a zároveň korigovať populáciu. Kľúčovou vlastnosťou tohto prístupu je, že ako výstup poskytuje minimálnu sadu génov, ktorá zachytáva gény, ktoré nesú kauzálne varianty s pravdepodobnosťou ρ. Prostredníctvom rozsiahlych simulácií sa demonštruje, že metóda nielen zrýchľuje výpočty, ale aj dosahuje v priemere o 10 % vyššiu mieru návratnosti v porovnaní s existujúcimi prístupmi. Metóda bola validovaná pomocou reálnych údajov o lipoproteínoch s vysokou hustotou (HDL) u myší a ukázalo sa, že CAVIAR-Gene je schopný identifikovať Apoa2 (gén známy ako nositeľ kauzálnych variantov pre HDL), pričom znižuje počet génov, ktoré je potrebné testovať na funkčnosť, dvakrát. Softvér je voľne dostupný na stiahnutie na genetics.cs.ucla.edu/caviar.
Vplyv genetických variácií na rast a vývoj
Eight independently isolated mutants which are supersensitive (Sst/sup -/) to the G1 arrest induced by the tridecapeptide pheromone ..cap alpha.. factor were identified by screening mutagenized Saccharomyces cerevisiae MATa cells on solid medium for increased growth inhibition by ..cap alpha.. factor. These mutants carries lesions in two complementation groups, sst1 and sst2. Mutations at the sst1 locus were mating type specific: MATa sst1 cells were supersensitive to ..cap alpha.. factor, but MAT..cap alpha.. sst1 cells were not supersensitive to a factor. In contrast, mutations at the sst2 locus conferred supersensitivity to the pheromones of the opposite mating type on bothmore » MATa and MAT..cap alpha.. cells. Even in the absence of added ..cap alpha.. pheromone, about 10% of the cells in exponentially growing cultures of MATa strains carrying any of three different alleles of sst2 (including the ochre mutation sst2-4) had the aberrant morphology (''shmoo'' shape) that normally develops only after MATa cells are exposed to ..cap alpha.. factor. This ''self-shmooing'' phenotype was genetically linked to the sst2 mutations, although the leakiest allele isolated (sst2-3) did not display this …
Osem nezávisle izolovaných mutántov, ktoré sú supersenzitívne (Sst/sup -/) na zastavenie v G1 fáze bunkového cyklu indukované tridekapeptidovým feromónom α-faktorom, bolo identifikovaných skríningom mutagénnych kvasinkových buniek Saccharomyces cerevisiae MATa na pevnom médiu pre zvýšenú inhibíciu rastu α-faktorom. Tieto mutanti nesú lézie v dvoch komplementačných skupinách, sst1 a sst2. Mutácie v lokuse sst1 boli špecifické pre párovací typ: bunky MATa sst1 boli supersenzitívne na α-faktor, ale bunky MATα sst1 neboli supersenzitívne na a-faktor. Naopak, mutácie v lokuse sst2 udelili supersenzitivitu na feromóny opačného párovacieho typu ako bunkám MATa, tak aj MATα. Dokonca aj v neprítomnosti pridaného α-feromónu, približne 10 % buniek v exponenciálne rastúcich kultúrach kmeňov MATa nesúcich akúkoľvek z troch rôznych alel sst2 (vrátane ochrovej mutácie sst2-4) malo aberantnú morfológiu ("shmoo" tvar), ktorá sa normálne vyvíja až po expozícii buniek MATa α-faktoru. Tento fenotyp "self-shmooing" bol geneticky spojený s mutáciami sst2, hoci najviac "pretekajúca" alela (sst2-3) nevykazovala tento…